 La matière:
Analyse immediate
La matière:
Analyse immediate
Logiciels et bibliographie
Programme d'étude
Cours
La matière
- Température
- Etats de la matières
- Types de corps
- Nomenclature*
- Mélanges
- Solutions
- Analyse immédiate
- Exercices
Un des problèmes de la chimie et de l'industrie est celui de la séparation des constituants d'un mélange. Ceci pour obtenir des produits utiles. Cette opération se nomme analyse immédiate.
Ces techniques de séparation sont des procédés physiques qui ne changent pas la nature des constituants. Il est cependant parfois nécessaire d'effectuer au préalable une transformation chimique d'un constituant avant de le séparer des autres, ceci pour que ses propriétés physiques soient mieux différenciées.
Exemple: Le silicium pour l'électronique doit être d'une très grande pureté. Pour ceci plusieurs étapes sont nécessaires.
Tamisage
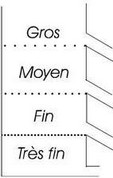 |
Cette méthode permet d'isoler un constituant solide d'une dimension déterminée dans un mélange. La séparation se fait à l'aide d'un tamis dont la dimension des trous est appropriée. Exemple: Séparation granulométrique des graviers. |
Filtration
 |
Il est possible d'isoler des particules solides d'un mélange solide-liquide ou solide-gaz en les retenant dans une matière poreuse. De nombreuses variantes existent. Exemples: Filtration de l'eau, analyse des poussières dans l'air. |
Sédimentation
Les particules solides ou liquides en suspension dans un liquide peuvent "tomber" sous l'action de leur poids. On utilise alors le terme de sédimentation. (Aussi décantation dans le cas solide-liquide)
Exemples:
Bassin à
sédimentation dans les STEP.
Lait-crème. Sang
(vitesse de sédimentation......).
Centrifugation
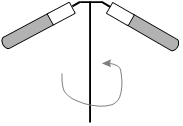 |
On peut accélérer la sédimentation en appliquant une force. Exemple: Centrifugation du sang, du lait, de certains virus etc... |
Fusion partielle
Utilisée lorsque dans un mélange de plusieurs solides, l'un des constituants a un point de fusion (P.F.) nettement inférieur aux P.F. des autres constituants. Il est alors possible de fondre un seul constituant.
Exemple: Extraction du soufre de la roche mère.
Evaporation
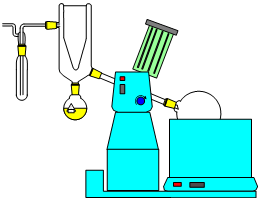 |
Dans une solution, il est possible d'évaporer le solvant et de récupérer le solide qui y était dissous. Exemple: Extraction du sel marin. |
Distillation
 |
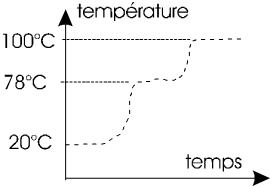 |
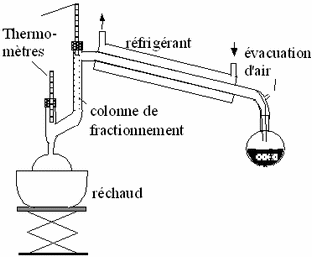
Elle permet de séparer des liquides de points d'ébullition (P.E.) différents dans un mélange, ceci par chauffage à ébullition et condensation des vapeurs. Cette méthode est très utilisée dans la pratique.
Lorsqu' on chauffe lentement un mélange de plusieurs liquides de P.E. différents, le liquide le plus volatil se met à bouillir en premier. Par condensation de la vapeur obtenue, on peut isoler le liquide le plus volatil. Souvent cette méthode n'est pas suffisante car une partie de l'autre constituant est entraînée par la vapeur du plus volatil. Il faut alors faire plusieurs distillations successives. Ceci est aussi possible au cours d'une distillation fractionnée effectuée dans une colonne à plateaux. Le parcours suivi par la phase vapeur est alors long et tortueux ce qui améliore la séparation.
Exemple:
Purification de divers
liquides
Eau de vie: on distille un mélange
eau+alcool (+purée de fruits), on récolte par
condensation l'alcool et on continue jusqu'à obtenir un
certain pourcentage d'eau.
Sublimation
Certains solides sont capables de passer directement de l'état solide à l'état gazeux. Il est possible de mettre à profit cette particularité pour séparer un constituant solide par chauffage et condensation de sa vapeur sous forme de solide directement.
Exemple: Purification de l'iode.
Extraction
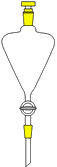 |
Il est possible d'extraire à l'aide de solvant un constituant solide ou liquide et de le récupérer ensuite par évaporation du solvant. Exemple: Extraction par de l'eau du sel de certaines roches. |
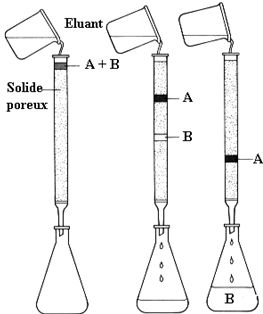
Chromatographie