 Stœchiométrie -
Equation et réaction chimique
Stœchiométrie -
Equation et réaction chimique
Logiciels et bibliographie
Programme d'étude
Cours
Stœchiométrie
- Masse atomique et molaire
- Equation et réaction chimique
- Calculs avec les équations chimiques
- Calculs avec des solutions aqueuses
- Facteurs expérimentaux
- Analyse élémentaire*
- Calculs avec des gaz*
- Exercices*
Par exemple, quand on électrolyse de l'eau, celle-ci se transfrome en dioxygène et dihydrogène, on le représente par l'équation:
2 H2 (g) + O2 (g)
 2 H2O (g)
2 H2O (g)
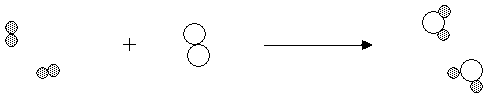
Les coefficients devant les substances servent à indiquer dans quelles proportions elles se trouvent.
Nous pouvons réaliser cette réaction à l'échelle macroscopique en respectant les proportions données par l'équation équilibrée.
2 H2 (g) +
O2 (g)
 2 H2O (g)
2 H2O (g)
2
molécules 1 molécule
2 molécules
échelle moléculaire
Multiplions par NA:
2 moles
1
mole
2 moles
échelle macroscopique
4
g
32
g
36 g
quantités stœchiométriques
- (s) pour solide
- (l) pour liquide
- (g) pour gazeux
- (aq) pour une solution de la substance avec l'eau comme solvant.