 Les éléments:
Tableau périodique
Les éléments:
Tableau périodique
Logiciels et bibliographie
Programme d'étude
Cours
Les éléments
- Masse
- Ondes
- Structure électronique
- Structure électronique moderne*
- Tableau périodique
- Electronégativité
- Taille des éléments
- Famille et éléments
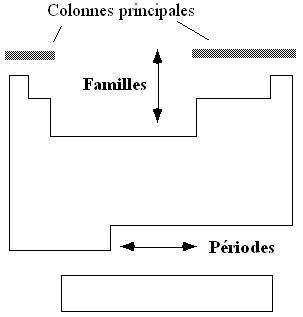 |
En 1869 Mendeleïev
montra que la série des éléments, classés par
nombre de protons croissant, peut se partager en tranches horizontales
appelées périodes.
Ceci de telle manière que les colonnes verticales appelées groupes ou familles renferment
des éléments ayant des propriétés analogues.
Cette manière d'arranger a pu par la suite s'expliquer par la structure électronque des atomes. En effet, dans une même colonne les propriétés sont analogues car une colonne contient des éléments ayant même nombre d'électrons sur la couche externe, qui est la plus importante pour les propriétés chimiques. Le nombre d'électrons sur cette couche correspond au numéro de la colonne pour les colonnes principales. |
Comme l'arrangement des éléments dans le tableau n'est pas dû au hasard, un grand nombre de propriétés d'un élément peuvent être déduites de son emplacement dans le tableau.
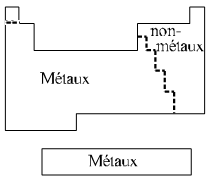 |
On distingue deux classes d'éléments dans le tableau périodique:
On appelle parfois métalloïdes un certain nombre d'éléments proche de la limite entre métaux et non-métaux. Le caractère métallique diminue de gauche à droite. |
Les éléments métalliques ont des
propriétés communes:
- Eclat métallique.
- Conductibilité électrique et thermique.
- Malléabilité, ductilité.
- Solide à température ambiante sauf le Hg.
Les éléments non-métalliques ont moins de similitudes dans leurs propriétés
On divise souvent le tableau périodique en blocs*:
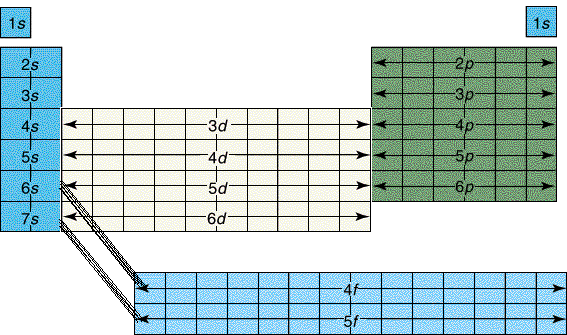 |
Ces blocs correspondent au
remplissage des sous couches électroniques spdf. Bloc d: éléments de transition Bloc f: terres rares N.B. 3d ne se trouve pas à la suite de 3s car 4s est de niveau énergétique plus bas que 3d (voir chapitre précédent) |
Exercice 1: Donner
les symboles pour les deux atomes suivants:
a) 11 protons, 12 neutrons, 11 électrons
b) 35 protons, 45 neutrons, 35 électrons 
Exercice
2*: Identifier la période et la famille de
chaque
élément ayant la configuration électronique
suivante des électrons de valence:
a) ns2 np3
b) ns1

Exercice
3: 1.
Déterminer s'il s'agit d'un métal, non-métal ou métalloïde:
a) Li c) B
e) La g) As
b) Si d) Cs
f) Mg h) S 